Arbeitsblatt: Chemische Zeichensprache
Material-Details
Einführung in die chemische Zeichen- und Formelsprache
Chemie
Chem. Formeln / Stöchiometrie
8. Schuljahr
2 Seiten
Statistik
31782
4603
48
04.01.2009
Autor/in
manne17 (Spitzname)
Land: Deutschland
Registriert vor 2006
Textauszüge aus dem Inhalt:
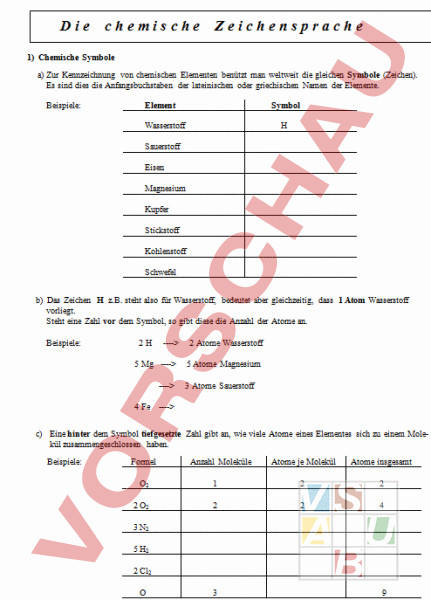
Die chemische Zeichensprache 1) Chemische Symbole a) Zur Kennzeichnung von chemischen Elementen benützt man weltweit die gleichen Symbole (Zeichen). Es sind dies die Anfangsbuchstaben der lateinischen oder griechischen Namen der Elemente. Beispiele: Element Symbol Wasserstoff Sauerstoff Eisen Magnesium Kupfer Stickstoff Kohlenstoff Schwefel b) Das Zeichen z.B. steht also für Wasserstoff, bedeutet aber gleichzeitig, dass 1 Atom Wasserstoff vorliegt. Steht eine Zahl vor dem Symbol, so gibt diese die Anzahl der Atome an. Beispiele: 2H ---- 2 Atome Wasserstoff 5 Mg ---- 5 Atome Magnesium ---- 3 Atome Sauerstoff 4 Fe ---- c) Eine hinter dem Symbol tiefgesetzte Zahl gibt an, wie viele Atome eines Elementes sich zu einem Molekül zusammengeschlossen haben. Beispiele: Formel Anzahl Moleküle Atome je Molekül Atome insgesamt O2 1 2 2 2 O2 2 2 4 3 N2 5 H2 2 Cl2 3 9 2) Chemische Formel Die chemische Formel gibt an, wie ein Stoff aufgebaut ist, das heißt, wie die kleinsten Teilchen (Atome, Moleküle) des Stoffes beschaffen sind. a) Bei Elementen kann man aus der Formel entnehmen, ob die kleinsten Teilchen Atome oder Moleküle sind, bzw. muss dieses beim Aufstellen einer Formel berücksichtigt werden. Beispiele: Element Formel Magnesium Mg Sauerstoff O2 Stickstoff Fe Cl2 Kupfer b) Bei Verbindungen kann man der Formel entnehmen, welche Elemente sich zu einem neuen Stoff, der Verbindung, zusammengeschlossen haben. Beispiele: Verbindung Formel Eisensulfid FeS Wasser H2O Kohlendioxid Al2O3 3) Wertigkeit Wenn wir eine Formel einer Verbindung aufstellen, dürfen wir jedoch nicht einfach die Symbole der in der Verbindung vorkommenden Elemente hintereinander schreiben. Viele Atome können nicht nut ein, sondern zwei oder noch mehr andere Atome an sich binden. Diese Eigenschaft nennt man Wertigkeit. Beim Aufstellen einer Formel ist nun also zu beachten, dass die Wertigkeiten der Elemente, die sich verbinden, summenmäßig gleich sind. Es kann sich demnach z.B. 1 zweiwertiges Element mit 2 einwertigen oder 1 zweiwertigen Element verbinden. Beispiele: a) HI und OII b) HI und NIII ---- NH3 c) AlII und OII ---- d) CIV und HI ---- e) MgII und ClI ---- f) AlIII und CIV ---- ---- H2O